氧气是人类生存的必需品,肺是人类接收氧气的主要器官,氢气是保护肺的重要工具!
人类呼吸的本质是周围环境系统和体内循环系统之间的气体交换:呼吸时,肺部是暴露在各种环境刺激物中的,包括细菌、病毒和其他病原体以及各种有害物质,如烟草颗粒、雾霾颗粒物等,短期或长期的有害物质通常会导致肺部损伤,造成各类肺部疾病。【1】
人类吸入空气时,细菌、病毒等有害物质一同进入体内
最初氢氧混合吸入概念的提出,是为了替代氦氧吸入——氦氧混合可以在临床上降低气道阻力,有利于氧气进入肺泡缓解呼吸困难等症状,而氢气同样具备“携氧弥散”的特性,且氢气同样对人体无害、氢气比氦气更易得···随着全球氢氧医学的发展,科学家发现大量氢氧吸入改善肺部疾病的证据,以下是中国医科大学盛京医院研究者整理的氢分子对肺部疾病的作用【2】。
一、氢分子抗氧化
在正常情况下,自由基的氧化还原反应对于免疫系统、信号传导、能量传递等方面非常重要,然而如果自由基的“量”太大,超过自身抗氧化能力,或者本身抗氧化能力下降,会导致氧化应激反应发生。通常,急性氧化应激多伴随炎症或缺血再灌注(I/R)一起发生(例如心脏骤停、心梗、脑梗、器官移植、手术止血等),慢性氧化损伤可发生在癌症、糖尿病、动脉粥样硬化、神经退行性病变等慢性炎症类疾病期间以及衰老期间。
这个时候机体可以通过抗氧化剂解决这些困扰,然而抗氧化剂又有很多种,目前发现氢分子的分子量低于其他常见的抗氧化剂,这让氢分子可以轻松穿过细胞膜、甚至细胞核膜、细胞线粒体膜,却不影响正常的代谢氧化还原反应,只选择性地与强氧化剂反应,在不影响细胞正常运转的情况下,解决氧化应激问题。同时,科学家还发现:氢分子可以刺激调节基因表达,促进抗氧化酶的表达,提升抗氧化酶SOD、CAT、MPO的活性,通过阻断凋亡信号调节激酶1(ASK1)信号通路和下游信号分子,从而抑制氧化酶的活性,降低自由基的产生。【3】
总结:氢分子抗氧化优势:1、分子量小可以穿透各种细胞膜,只和强氧化剂发生作用,不影响正常氧化还原反应;2、通过基因表达、信号调节等,增强“联军”抗氧化酶的产生,并提升活性;3、抑制“敌军”氧化酶的活性,并减少自由基的生成。
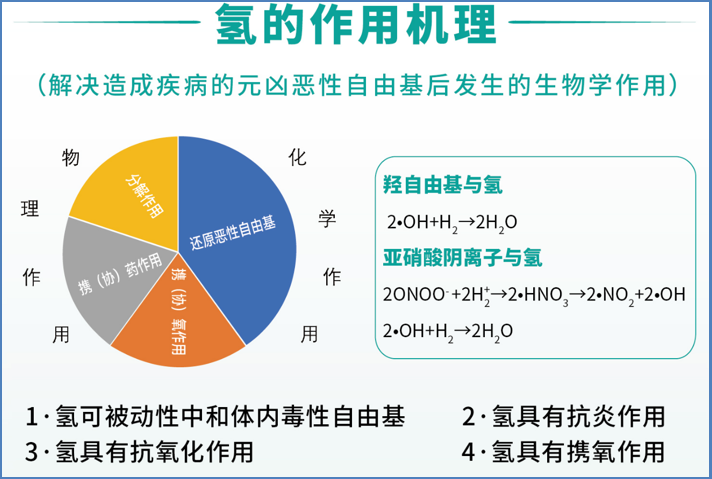
氢的作用机理
二、氢分子抗炎
氢分子对多种肺部疾病(包括慢阻肺、哮喘、肺纤维化、肺损伤等)的改善作用也是基于氢的抗炎性特点。氢分子对炎症反应的作用是多角度、多层面共同起作用的,具体如下:
1、氢分子能抑制促炎因子TNF-α、IL-1β、IL-6、NF-κB、HMGB-1的合成和释放,增加抗炎因子IL-10的表达;2、氢分子可以抑制细胞间黏附分子-1(ICAM-1)、粒细胞-巨噬细胞集落刺激因子(GMCSF)、粒细胞集落刺激因素(G-CSF)的释放;3、氢分子可以促进病变部位巨噬细胞吞噬细胞增多、并抑制中性粒细胞和M1巨噬细胞向病变发展;4、氢分子参与到信号通路如:Nrf2/HO-1/HMGB-1通路的刺激减轻由微生物败血症引起的内皮功能障碍和肺损伤;p38MAPK和c-Jun N-末端激酶(JNK)的抑制减轻了LPS诱导的急性肺损伤(ALI);通过哺乳动物雷帕霉素靶点(mTOR)/转录因子EB(TFEB)和PTEN诱导的激酶1(PINK1)/Parkin通路,减轻急性肺损伤ALI内皮功能障碍和心肌缺血性再灌注损伤(I/R)等。【4】
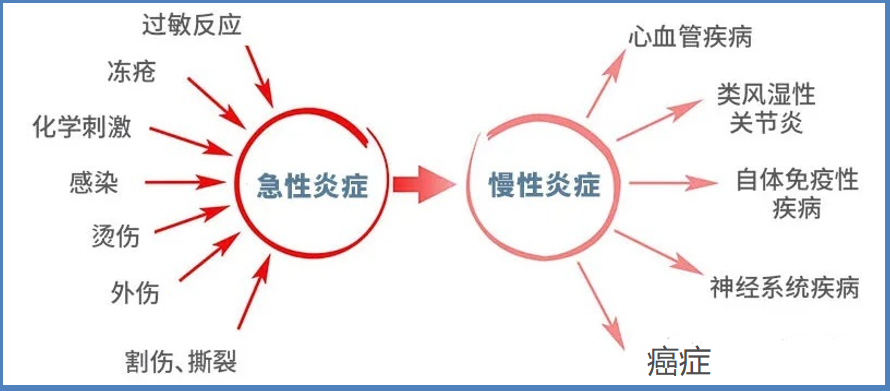
炎症和伤病
由上可知,氢分子对于炎症具有全方位抑制作用,这一过程可以减缓、改善肺部疾病的产生、发展。在过往研究中,很多肺部疾病实验对比了不同剂量的氢氧吸入情况,结果发现氢氧吸入具有明显“剂量效应”,最直接的证据是就是高剂量氢氧吸入组各项炎症指标的改善明显比低剂量组好很多。这些实验在本公众号可自行查看,因此不再赘述。
三、氢的自噬调节
自噬是对细胞非常重要的一个调节过程,自噬调节可以吞噬自身细胞蛋白或细胞器与溶酶体融合形成自噬溶酶体,降解内容物的过程,借此机体可以实现细胞本身的代谢和某些细胞器的更新换代。但自噬过度也会产生很多不良影响导致细胞损伤甚至死亡。新出现的证据表明氢分子对细胞自噬具有双向调节作用。【5】
1、氢分子促进自噬
氢分子可以促进巨噬细胞中自噬介导的核苷酸结合结构域和富含亮氨酸的重复蛋白3(NLRP3)失活,减轻炎症反应和气管损伤带来的线粒体功能障碍。在败血症中,内质网应激被激发,伴随自噬受损。氢通过激活自噬减轻内质网应激,从而减轻炎症和气管损伤,这些结果表明,氢气通过适当促进自噬来维持体内平衡、减轻压力的影响,从而保护机体。
2、氢分子抑制自噬
过度的自噬会破坏细胞稳态。在之前研究中,科学家已发现氢分子抑制过度自噬来减轻急性肺损伤,同时在创伤性脑损伤中,氢通过抑制自噬提高微血管内皮细胞生存能力。尽管氢分子进行自噬调节的机制尚待明确,但按照氢分子对于自噬的调节作用,氢分子在临床上也被视作调节自噬的方案之一。
四、氢调节细胞死亡
1、调控细胞凋亡
细胞凋亡是细胞程序性死亡的经典方式,正常的细胞凋亡对生物具有极大意义。细胞凋亡的分子机制包括半胱氨酸蛋白酶的激活、以及一系列促进凋亡和抗凋亡的B细胞淋巴瘤-2(Bcl-2)家组蛋白。在过去的氢氧医学研究中,科学家发现氢分子通过调节细胞凋亡来发挥保护作用——氢分子可以通过调节细胞凋亡信号通路和细胞凋亡相关蛋白来抑制细胞凋亡,比如磷脂酰肌醇-3-激酶(PI3K)/蛋白激酶B(Akt)/糖原合成酶激酶-3β(GSK3β)、ASK1/JNK、大鼠肉瘤(Ras)-细胞外信号相关激酶1/2(ERK1/2)-丝裂原活化蛋白激酶1/2(MEK1/2)和Akt途径,并通过抑制胱天蛋白酶-3、-8、-9的激活和Bcl-2/Bcl-2相关比率。
氢分子还可以通过抗炎症、抗氧化来减少细胞凋亡率并保护线粒体功能。在缺血再灌注(I/R)模型中,PINK介导的自噬减轻炎症和细胞凋亡。当然氢分子也有促进细胞凋亡的一面,比如有科学家发现氢分子可以促进癌症早期、晚期癌细胞的凋亡,减少癌细胞增殖,促进癌症细胞凋亡而死。因此,氢分子对凋亡的控制成为现代医学对抗慢性疾病(癌症)的重要选择。【6】
2、氢分子对细胞焦亡的调节
焦亡是一种新发现的与炎症相关的程序性细胞死亡。炎症小体中模式识别受体(PRRs)的激活可以通过刺激炎症反应触发细胞焦亡。细胞焦亡也是一种保护机制,但过度细胞焦亡会产生严重后果。ROS以及胱天蛋白酶-1和炎症小体的激活在促进焦亡中发挥重要作用。氢分子在抵抗炎症和氧化方面起着重要的调节作用。因此,氢可能影响炎症性疾病中的细胞焦亡,如败血症和I/R损伤。在大鼠心肌I/R损伤模型中,氢抑制氧化应激和NLRP3介导的细胞焦亡,并显著改善心脏功能、微观结构和线粒体形态。【7】
五、氢对抗衰老
我们对衰老很熟悉,衰老是不可避免的过程,最终会导致人的死亡。研究发现氢分子对于衰老的进度具有影响:氢分子可以降低和衰老有关的蛋白β-半乳糖苷酶、p53、p21的表达,抑制Sirt3表达下调,并减少氧化应激损伤从而延长细胞寿命···
研究表明,人体本身肠道细菌会产生氢气,这些氢分子通过抑制细胞内的·OH介导的脂质过氧化物形成和细胞衰老来抑制过氧化氢的增加,这有利于抑制机体的衰老。基因组不稳定是衰老的另一大原因,氢分子可以减轻DNA损伤,帮助维持基因组的稳定性从而改善衰老:例如在肺气肿研究中,氢分子显著降低磷酸化组蛋白H2AX和8-羟基-2-脱氧鸟苷(8-HHdG)——这是DNA氧化损伤标志物。综上,氢氧吸入被科学家认为具有抗衰老的潜力。【8】
氢可能产生的生物效应:
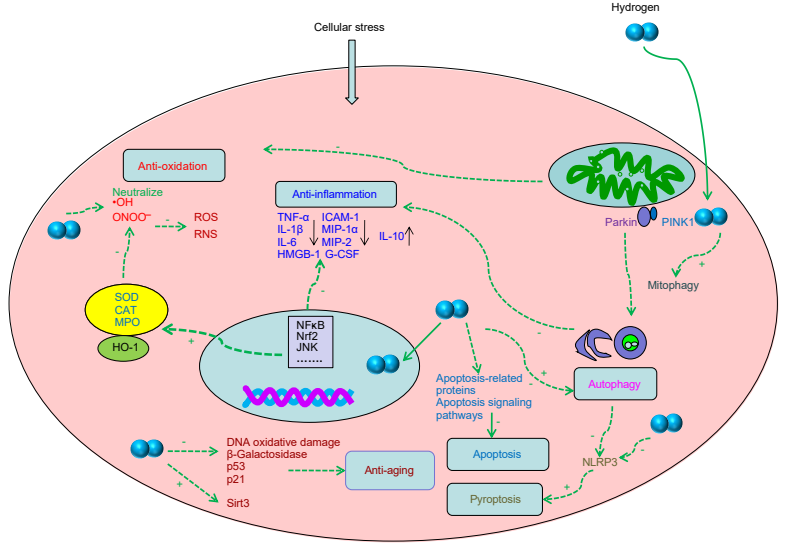
图中:氢通过直接中和·OH、上调Nrf2、HO-1、SOD、CAT和MPO以及清除ONOO来发挥抗氧化活性;氢通过抑制NF-κB和促炎因子(TNF-α、IL-1β、IL-6和HMGB-1),抑制MIP-1α、MIP-2、G-CSF和ICAM-1,并增加抗炎因子IL-10的表达来发挥抗炎活性;氢调节自噬,包括Parkin/PINK1介导的线粒体自噬,减轻炎症和NLRP3介导的焦下垂;氢通过调节凋亡相关蛋白和信号通路抑制细胞凋亡,但促进癌症细胞凋亡;氢通过减少DNA氧化损伤,降低衰老相关蛋白β-半乳糖苷酶、p53和p21的表达,并上调Sirt3的表达,具有抗衰老作用。
名词解释:+指激活;−指抑制。RNS:活性氮种类;ROS:活性氧;NF-κB:核因子-κB;JNK:c-Jun N-末端激酶·OH:羟基自由基;ONOO:过氧亚硝酸根阴离子;HO-1:血红素加氧酶-1;SOD:超氧化物歧化酶;CAT:过氧化氢酶;MPO:髓过氧化物酶;NLRP3:核苷酸结合结构域和富含亮氨酸的重复蛋白3;PINK:磷酸酶和紧张素同源物(PTEN)诱导的激酶;TNF-α:肿瘤坏死因子-α;G-CSF:粒细胞集落刺激因子;ICAM-1:细胞间粘附分子-1;IL:白细胞介素;HMGB-1:高移动性组盒1;MIP:巨噬细胞炎症蛋白;Sirt3:sirtuins 3;Nrf2:核因子-红系2相关因子2。
这篇研究也分别讲解了高浓度氢氧吸入对于慢阻肺、急性肺损伤、肺纤维化、支气管哮喘、新冠肺炎、过敏性鼻炎、睡眠呼吸障碍等多种呼吸疾病的改善情况,这些内容本公众号均进行过详细报道,可点击下列标题跳转阅读:
···
六、氢对肺的保护
氢对肺部疾病作用:
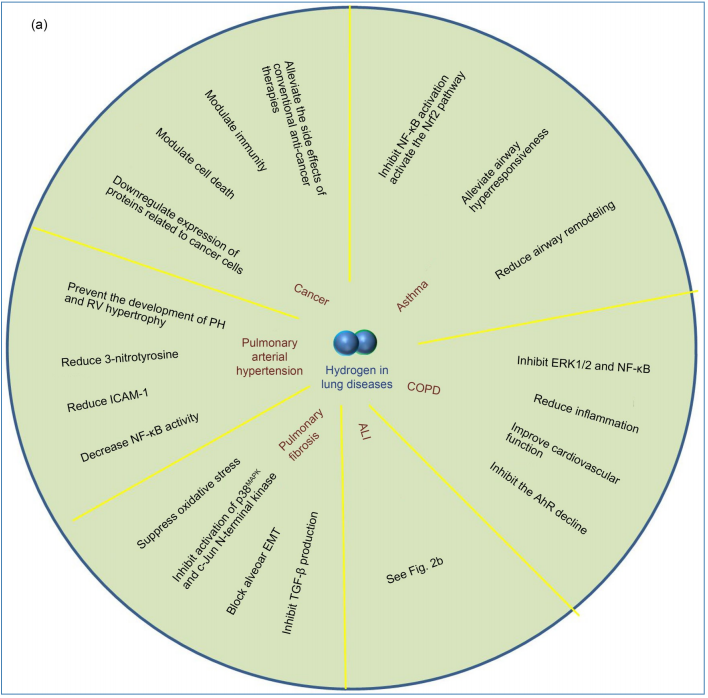
(a) 氢对各种肺部疾病具有保护和治疗作用,在COPD中,氢抑制ERK1/2和NF-κB,减少炎症,抑制与COPD发病机制相关的AhR下降,并改善心血管功能。在哮喘中,氢抑制NF-κB,激活Nrf2通路,并减少气道重塑。在癌症中,氢减轻了其他抗癌疗法的副作用,调节了免疫和细胞死亡,并抑制了癌症细胞相关蛋白的表达。在PAH中,氢减少3-硝基酪氨酸、ICAM-1和NF-κB,并防止PH和RV肥大的发展。在PF中,氢抑制氧化应激和炎症,并阻断肺泡EMT和TGF-β的产生。
氢分子对各类急性肺损伤(ALI)的作用:

氢对急性肺损伤ALI的影响。在LPS诱导的ALI中,氢抑制肺组织的炎症和细胞凋亡,并减少上皮和内皮功能障碍。在败血症诱导的ALI中,氢抑制HMGB-1,减少线粒体功能障碍,并与其他治疗发挥协同作用。在病毒诱导的ALI中,氢可能对治疗新冠肺炎有效。在I/R诱导的ALI中,氢抑制炎症和氧化应激,抑制肺组织凋亡,减轻肺移植和其他原因引起的肺损伤。氢还可以缓解由各种其他因素引起的ALI。
名词解释:COPD:慢性阻塞性肺病;ERK1/2:细胞外信号调节激酶1/2;NF-κB:核因子-κB;AhR:芳烃受体;Nrf2:核因子-红系2相关因子2;PAH:肺动脉高压;ICAM-1:细胞间粘附分子-1;PH:肺动脉高压;RV:右心室;PF:肺纤维化;EMT:上皮-间充质转化;TGF-β:转化生长因子-β;ALI:急性肺损伤;LPS:脂多糖;HMGB-1:高移动性组盒1;新冠肺炎:2019冠状病毒病;I/R:缺血/再灌注;VILI:呼吸机引起的肺损伤;HO-1:血红素加氧酶-1;MDA:丙二醛;SOD:超氧化物歧化酶;AQP:水通道蛋白。
七、总结
越来越多的研究表明氢分子具有广泛的生物效应,高浓度氢氧吸入是目前人类已知普遍应用到临床上,且未发现明显副作用的氢分子摄取途径。一方面氢氧结合避免了缺氧的可能性,另外氢氧同时吸入避免了“缺氧环境利于癌细胞移殖”的情况。上述氢分子调节氧化应激、炎症、自噬、程序性细胞死亡(凋亡、焦亡)、调节衰老等等,很清楚地讲述了氢氧在动物实验、临床实验中如何保护器官和系统。
本篇研究主要集中在氢氧对肺部疾病的改善,通过大量案例我们了解到,氢氧除了直接保护肺部以外,还通过对其他器官和组织的保护间接对肺部起到改善作用。按照目前的研究结论,再加上未来临床的不断推广验证,我们有信心将氢氧打造成人类战胜肺部疾病,乃至战胜衰老的有力武器!
参考资料:
【1】Bhattacharya J, Matthay MA, 2013. Regulation and repair of the alveolar-capillary barrier in acute lung injury. Annu Rev Phys, 75:593-615.
【2】Zhiling FU, Jin ZHANG,Molecular hydrogen is a promising therapeutic agent for pulmonary disease,Biomedicine & Biotechnology) 2022 23(2):102-122
【3】Cai WW, Zhang MH, Yu YS, et al., 2013. Treatment with hydrogen molecule alleviates TNFα-induced cell injury in osteoblast. Mol Cell Biochem, 373(1-2):1-9. https://doi.org/10.1007/s11010-012-1450-4
【4】Chen HG, Han HZ, Li Y, et al., 2020. Hydrogen alleviated organ injury and dysfunction in sepsis: the role of crosstalk between autophagy and endoplasmic reticulum stress: experimental research. Int Immunopharmacol, 78:106049.
【5】Wang YF, Wang L, Hu TP, et al., 2020. Hydrogen improves cell viability partly through inhibition of autophagy and activation of PI3K/Akt/GSK3β signal pathway in a micro ‐vascular endothelial cell model of traumatic brain injury. Neurol Res, 42(6):487-496
【6】Jiang Y, Liu G, Zhang L, et al., 2018. Therapeutic efficacy of hydrogen-rich saline alone and in combination with PI3K inhibitor in non-small cell lung cancer. Mol Med Rep,18(2):2182-2190.https://doi.org/10.3892/MMR.2018.9168
【7】Nie CQ, Ding X, A R, et al., 2021. Hydrogen gas inhalation alleviates myocardial ischemia-reperfusion injury by the inhibition of oxidative stress and NLRP3-mediated pyroptosis in rats. Life Sci, 272:119248.
【8】Sakai T, Kurokawa R, Hirano SI, et al., 2019. Hydrogen indirectly suppresses increases in hydrogen peroxide in cytoplasmic hydroxyl radical-induced cells and suppresses cellular senescence. Int J Mol Sci, 20(2):456.










